Conheça a Imunoterapia Dirgida às Células Dendríticas com Antígenos Glicoconjugados
CADASTRE-SE
Doenças alérgicas representam um problema de saúde pública, atingindo mais de 20% da população mundial. Estima-se que até 2030, 50% da população mundial terá algum tipo de manifestação alérgica.

... Entretanto, aderência permanece sendo um desafio. Entre os prováveis motivos estão a longa duração do tratamento e o grande número de doses necessárias para atingir a eficácia clínica.

Desta forma, os antígenos glicoconjugados emergem como uma alternativa mais eficiente aos antígenos nativos.
Beneficiam-se das Células Dendríticas atuarem na indução de tolerância para iniciar e manter as repostas imunes
Na glicoconjugação, adjuvantes baseados em carboidratos ou polissacarídeos são conjugados à proteínas especificas.
As proteínas dos ácaros, por exemplo, são conjugadas às moléculas de açúcar.
Essa Imunoterapia passa então a ser dirigida aos receptores de carboidratos específicos da familia das Lectinas C (CLRs) presents nas Dcs
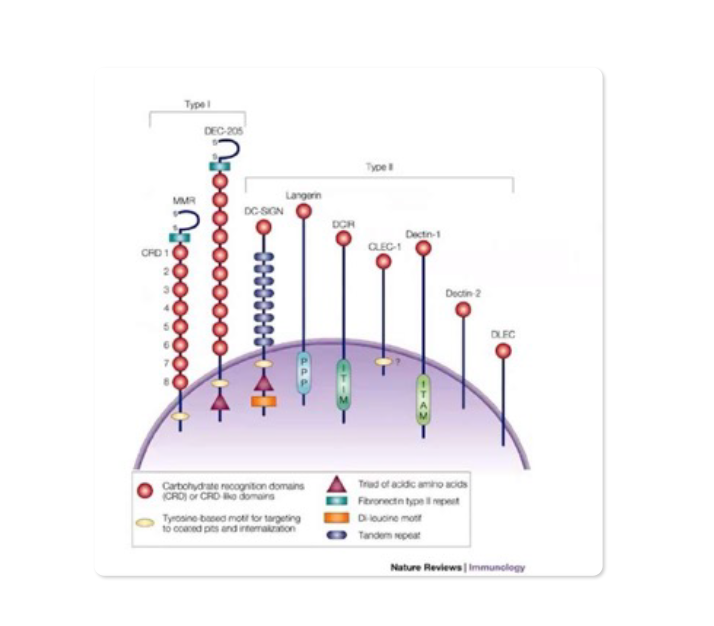
Ação imunoestimulante e de sistema vetor de entrega
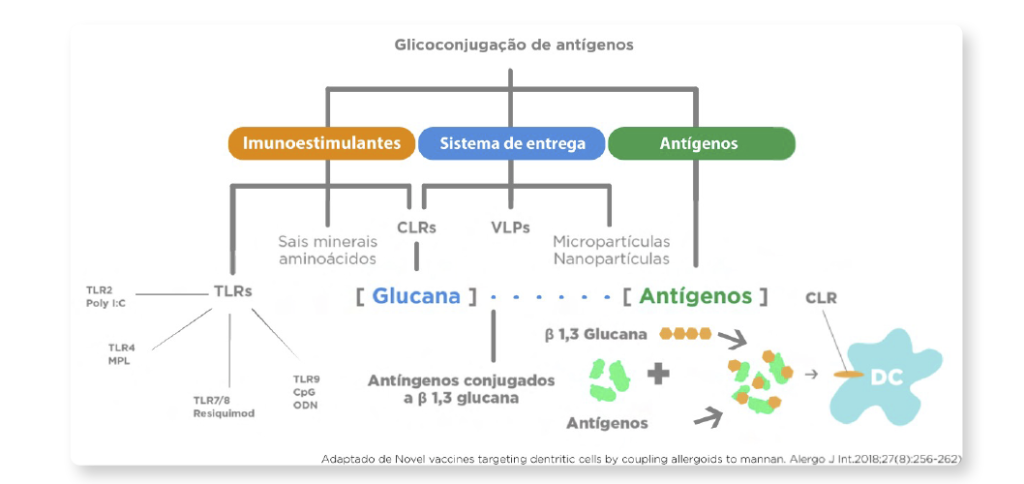
A glicoconjugação de antígenos (S. Cerevisiae) aumenta a biodisponibilidade, facilita a absorção de antígenos e promove maior indução de células T reguladoras e melhora o perfil de segurança conforme podemos ver a seguir

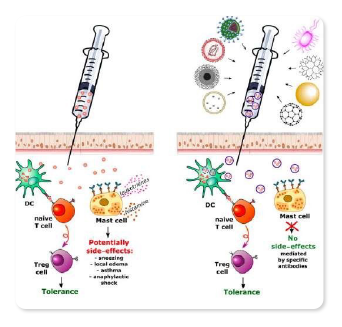
A retirada do Gel de Hidróxido de Alumínio, reduz a degradaçào de proteinas e aumenta a tolerogênicidade das formulações. Melhora o perfil de segurança com menor nível de respostas TH2
Estudos internacionais demonstram que os antígenos glicoconjugadas são mais eficazes, mais convenientes do que as imunoterapias com antígenos nativos.
Melhoram a eficácia da imunoterapia alérgeno específica e otimizam os protocolos com doses em média a cada 5 semanas.

Novas Formulações (Aéroalergenos)
AC – ÁCAROS MIX
98% Ácaros (D. pteronyssinus, B. tropicalis, D. Farinae) + 2% Betaglucana
AM – ÁCAROS + MOSQUITOS MIX
98% (Ácaros + Mosquito Mix)+ 2% Betaglucana
FOM – FORMIGAS MIX
98% (Solenopsis invicta (Formiga Lava-pés Vermelha) + Solenopsis richteri + 2% Betaglucana
AE – ÁCAROS + EPITÉLIOS MIX
98% (Ácaros Mix + Epitélios)+ 2% Betaglucana
Referências Bibliográficas:
Bousquet J, Grattan CE, Akdis CA, Eigenmann PA, Hoffmann-Sommergruber K, Agache I, Jutel M. Highlights and recent developments in allergic diseases in EAACI journals (2019). Clin Transl Allergy. 2020 Dec 3;10(1):56. doi: 10.1186/s13601-020-00366-3. PMID: 33292572; PMCID: PMC7712618.
Malling HJ. WHO-Positionspapier (Kurzfassung)–Allergen-Immuntherapie: therapeutische Impfstoffe für allergische Krankheiten [WHO position paper (summary)–allergen-immunotherapy: therapeutic vaccines for allergic diseases]. Wien Med Wochenschr. 1999;149(14-15):410-4. German. PMID: 10584284.
Bousquet J, Grattan CE, Akdis CA, Eigenmann PA, Hoffmann-Sommergruber K, Agache I, Jutel M. Highlights and recent developments in allergic diseases in EAACI journals (2019). Clin Transl Allergy. 2020 Dec 3;10(1):56. doi: 10.1186/s13601-020-00366-3. PMID: 33292572; PMCID: PMC7712618.
4.JutelM,AgacheI,BoniniS,BurksAW,CalderonM,Canonica W, etal. International Consensus onAllergenImmunother-apy II: mechanisms, standardization, and pharmacoeco-nomics. J Allergy Clin Immunol. 2016;137:358–68
5. Benito-Villalvilla C, Soria I, Subiza JL, Palomares Novel vaccines targeting dendritic cells by coupling allergoids to mannan. Allergo J Int. 2018;27(8):256-262
6. Benito-Villalvilla C, Soria I, Pérez-Diego M, Fernández-Caldas E, Subiza JL, Palomares Alum impairs tolerogenic properties induced by allergoid-mannan conjugates inhibiting mTOR and metabolic reprogramming in human DCs. Allergy. 2020 Mar;75(3):648-659.
Benito-Villalvilla C, Pérez-Diego M, Angelina A, Kisand K, Rebane A, Subiza JL, Palomares O. Allergoid-mannan conjugates reprogram monocytes into tolerogenic dendritic cells via epigenetic and metabolic rewiring. J Allergy Clin Immunol. 2022 Jan;149(1):212-222.e9.
8. Soria I, Alvarez J, Manzano AI, López-Relaño J, Cases B, Mas-Fontao A, Cañada FJ, Fernández-Caldas E, Casanovas M, Jiménez-Barbero J, Palomares O, Viñals-Flórez LM, Subiza Mite allergoids coupled to nonoxidized mannan from Saccharomyces cerevisae efficiently target canine dendritic cells for novel allergy immunotherapy in veterinary medicine. Vet Immunol Immunopathol. 2017 Aug;190:65-72.
9 Manzano AI, Javier Cañada F, Cases B, Sirvent S, Soria I, Palomares O, Fernández-Caldas E, Casanovas M, Jiménez-Barbero J, Subiza JL. Structural studies of novel glycoconjugates from polymerized allergens (allergoids) and mannans as allergy vaccines. Glycoconj J. 2016 Feb;33(1):93-101.
10. Sirvent S, Soria I, Cirauqui C, Cases B, Manzano AI, Diez-Rivero CM, Reche PA, López-Relaño J, Martínez-Naves E, Cañada FJ, Jiménez-Barbero J, Subiza J, Casanovas M, Fernández-Caldas E, Subiza JL, Palomares Novel vaccines targeting dendritic cells by coupling allergoids to nonoxidized mannan enhance allergen uptake and induce functional regulatory T cells through programmed death ligand 1. J Allergy Clin Immunol. 2016 Aug;138(2):558-567.e11.
11. Schülke S, Vieths Dendritic cell targeting with C-type lectins for improvement of allergen immunotherapy. J Allergy Clin Immunol. 2016 Aug;138(2):568-70.
12. González JL, Zalve V, Fernández-Caldas E, Cases B, Subiza JL, Casanovas M. A pilot study of immunotherapy in dogs with atopic dermatitis using a mannan-Dermatophagoides farinae allergoid targeting dendritic cells. Vet Dermatol. 2018 Oct;29(5):449-e152.
13. Sánchez-Ramón S, Conejero L, Netea MG, Sancho D, Palomares Ó, Subiza Trained Immunity-Based Vaccines: A New Paradigm for the Development of Broad-Spectrum Anti-infectious Formulations. Front Immunol. 2018 Dec 17;9:2936
Cirauqui C, Benito-Villalvilla C, Sánchez-Ramón S, Sirvent S, Diez-Rivero CM, Conejero L, Brandi P, Hernández-Cillero L, Ochoa JL, Pérez-Villamil B, Sancho D, Subiza JL, Palomares O. Human dendritic cells activated with MV130 induce Th1, Th17 and IL-10 responses via RIPK2 and MyD88 signalling pathways. Eur J Immunol. 2018 Jan;48(1):180-193.
Brandi P, Conejero L, Cueto FJ, Martínez-Cano S, Dunphy G, Gómez MJ, Relaño C, Saz-Leal P, Enamorado M, Quintas A, Dopazo A, Amores-Iniesta J, Del Fresno C, Nistal-Villán E, Ardavín C, Nieto A, Casanovas M, Subiza JL, Sancho D. Trained immunity induction by the inactivated mucosal vaccine MV130 protects against experimental viral respiratory infections. Cell Rep. 2022 Jan 4;38(1):110184.
Nieto A, Mazón A, Nieto M, Calderón R, Calaforra S, Selva B, Uixera S, Palao MJ, Brandi P, Conejero L, Saz-Leal P, Fernández-Pérez C, Sancho D, Subiza JL, Casanovas M. Bacterial Mucosal Immunotherapy with MV130 Prevents Recurrent Wheezing in Children: A Randomized, Double-Blind, Placebo-controlled Clinical Trial. Am J Respir Crit Care Med. 2021 Aug 15;204(4):462-472.
Martin-Cruz L, Sevilla-Ortega C, Benito-Villalvilla C, Diez-Rivero CM, Sanchez-Ramón S, Subiza JL, Palomares O. A Combination of Polybacterial MV140 and Candida albicansV132 as a Potential Novel Trained Immunity-Based Vaccine for Genitourinary Tract Infections. Front Immunol. 2021 Jan 21;11:612269.
Benito-Villalvilla C, Cirauqui C, Diez-Rivero CM, Casanovas M, Subiza JL, Palomares O. MV140, a sublingual polyvalent bacterial preparation to treat recurrent urinary tract infections, licenses human dendritic cells for generating Th1, Th17, and IL-10 responses via Syk and MyD88. Mucosal Immunol. 2017 Jul;10(4):924-935.
Baert K, De Geest BG, De Greve H, Cox E, Devriendt B. Duality of β-glucan microparticles: antigen carrier and immunostimulants. Int J Nanomedicine. 2016 May 31;11:2463-9. doi: 10.2147/IJN.S101881. PMID: 27330289; PMCID: PMC4898424.




